Biomedical Optics Express丨Laser induced forward transfer isolating complex-shaped cell by beam shaping
2021.10.21
摘要
2021年10月,中科院长春光机所李备研究员团队,在期刊《Biomedical Optics Express》上发表文章“Laser induced forward transfer isolating complex-shaped cell by beam shaping”。

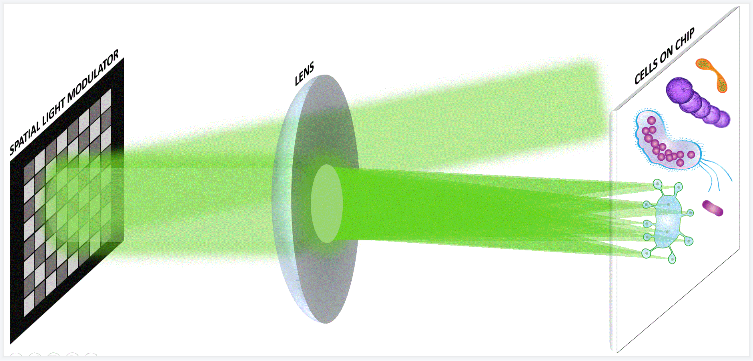
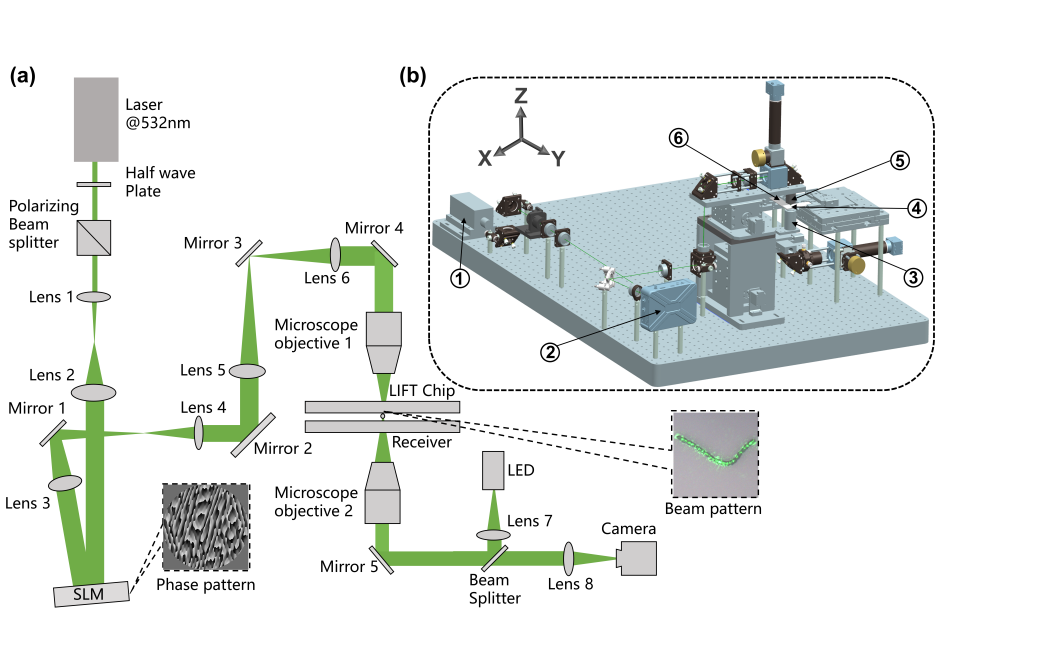
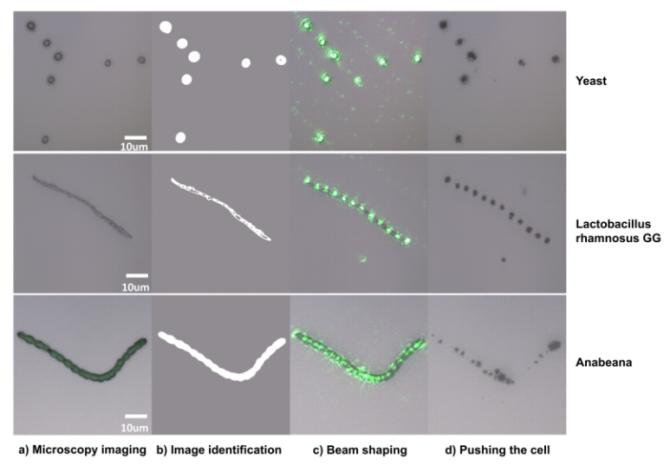
该工作基于激光诱导向前转移技术,结合图像识别与光束整形技术,实现了对于复杂形态、不同大小的微生物细胞(丝状菌、鞭毛虫等)的单细胞弹射分选。作为长光辰英核心产品——PRECI SCS单细胞分选仪的技术升级,目前可分选微生物尺寸从500nm-100μm,极大扩展了该技术可分选细胞的尺寸范围,此外该技术亦可同时分选多个单细胞,为单细胞高通量分选奠定基础,更好地满足不同单细胞分选的研究。
01
研究背景
02
图文导读
03
结论